Все больше людей в мире умирает от хронических неинфекционных болезней (диабет, онкологические и сердечно-сосудистые заболевания). Что же способно остановить подобную эпидемию? Ответ даст нутригеномика — новое направление в науке, изучающее, как пища влияет на экспрессию генов. Cтатья раскроет молекулярные механизмы воздействия пищи на гены; расскажет о том, какие продукты стоит употреблять чаще, а от каких отказаться, чтобы жить дольше и здоровее; и опишет перспективы диетологии в будущем.
Еще со времен Древней Греции было известно, что пища влияет на состояние тела и духа и способна избавлять от болезней. Однако фундаментальные открытия в науке о питании были сделаны только в 18–20 столетиях: изучили химический состав пищи и основные пути метаболизма [1]. До середины 20 века из-за несбалансированного рациона были распространены недуги, связанные с дефицитом витаминов и минералов, поэтому их функции исследовались особенно активно. Сегодня же развитые страны столкнулись с другими последствиями нерационального питания — ожирение и диабет II типа [2] (рис. 1). Более того, обнаружено, что продолжительность жизни и развитие «убийственной тройки» — сердечно-сосудистых, нейродегенеративных и раковых заболеваний — зависит от рациона человека [3]. Медикам и ученым стало очевидно, что для эффективного лечения и профилактики вышеупомянутых заболеваний необходимо понять механизмы воздействия пищи на организм на клеточном и молекулярном уровнях. В начале 21 века завершились международные геномные проекты [4], предоставив для анализа множество генетической информации; стали развиваться производительные молекулярные методы для исследования «внутренней жизни» клетки [5]. Все эти факторы привели к рождению новой науки — нутригеномики [6].
Нутригеномика исследует влияние различных компонентов пищи и биологически активных добавок на экспрессию генов [7]. Ожидается, что определение биохимических путей взаимодействия пищи и генов позволит эффективно лечить неинфекционные заболевания (например, диабет, рак, патологии сердечно-сосудистой системы), а также предотвращать их развитие благодаря выявлению ранних маркеров нарушений в метаболизме и составлению индивидуального плана питания [6].
Каким же образом пища регулирует работу генов?
Нутригеномика: от пищи к генам
Экспрессия генов — это процесс, в ходе которого наследственная информация от гена преобразуется в функциональный продукт — РНК или белок. Экспрессия генов регулируется на разных стадиях, но главный «контрольный пункт» — это начало транскрипции (синтеза РНК на матрице ДНК). Инициация транскрипции зависит как от наличия необходимых белков (транскрипционные факторы, ферменты и пр.), так и от доступности (сродства) ДНК для этих белков (т.е. от эпигенетических модификаций). Компоненты пищи способны влиять на оба процесса [6, 7].
Эпигенетические модификации
Все клетки нашего организма — от нейронов до лейкоцитов — несут одинаковый генетический материал. Но в каждой клетке экспрессируется специфический набор генов — это определяет специализацию клеток. Включение/выключение генов регулируется эпигенетическими модификациями (такие модификации не затрагивают последовательность ДНК, но меняют ее «обвеску»). В клетке ДНК компактизирована, т.е. намотана на «бусины» — комплекс белков гистонов, различные химические модификации которых включают или выключают ген. Помимо этого, выключение генов происходит при модификации непосредственно молекулы ДНК (метилирование).
Некоторые компоненты пищи влияют на эти процессы (рис. 2):
- Ацетилирование гистонов (включение гена). Сульфарафан (содержащийся в капусте, брокколи, цветной капусте) и диаллилдисульфид (из чеснока) — включают гены, подавляя ферменты, которые репрессируют ген посредством снятия ацетильной метки с гистонов. Поэтому сульфарафан способен включать молчащие в раковых клетках гены — регулировщики нормального деления, что подавляет рост опухоли. Масляная кислота, которая образуется микрофлорой человека при употреблении клетчатки, оказывает аналогичное влияние на работу генов, а также активирует иммунную систему, что подавляет рост раковых клеток. Ингибирующее действие масляной кислоты на метастазирование было показано у крыс на модели рака прямой кишки [8].
Метилирование ДНК (выключение гена). Источники метильных групп (холин, метионин, фолиевая кислота) содержатся в яйцах, шпинате, бобовых и печени. У взрослых крыс хронический дефицит метильных групп влечет за собой спонтанное образование опухолей [9], а также ведет к активации мобильных элементов генома [10]. Широко известен эксперимент, проведенный Джиртлом и Уотерлэндом, с трансгенными грызунами агути (Avy agouti), которые имеют желтую окраску и предрасположенность к ожирению, диабету и раку. При добавлении в корм беременным самкам агути холина, метионина и фолиевой кислоты у них рождалось нормальное потомство с коричневой окраской шерсти и без отклонений в здоровье [11]. Дело в том, что присутствие источников метильных групп в пище матери способствовало метилированию (и, соответственно, выключению) гена agouti, вызывавшего болезненный фенотип у эмбрионов*.
* — Подробнее про то, как эпигенетические модификации влияют на развитие читайте в «Развитие и эпигенетика, или история о минотавре», «Эпигенетика: невидимый командир генома» [12, 13].
Для нормального развития плода и протекания беременности у женщин необходимы источники метильных групп, в частности, фолиевая кислота. При ее дефиците повышается риск преждевременных родов, выкидышей, а также возможны патологии в нервной системе плода и низкий вес новорожденного [14]. Точные механизмы действия фолиевой кислоты до сих пор не ясны, известно лишь, что усиливается метилирование гена IGF2 (инсулиноподобного фактора роста 2), участвующего в росте и развитии плода[15].
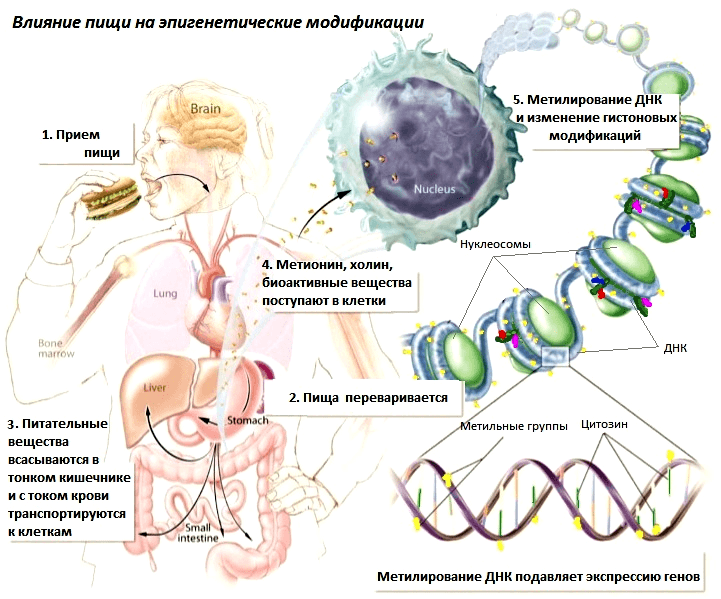
Рисунок 2. Механизм влияния пищи на эпигенетические модификации. Рисунок c сайта epigeek.com.
Транскрипционные факторы
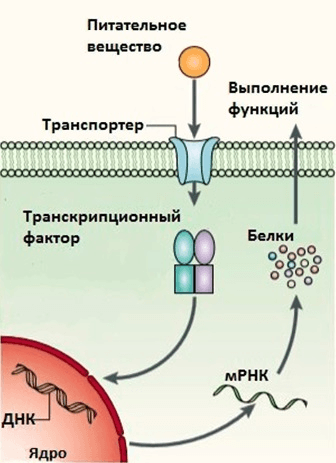
Рисунок 3. Механизм действия нутриентов на экспрессию генов через транскрипционные факторы. Рисунок из [6], адаптирован.
Второй механизм, посредством которого пища изменяет экспрессию генов, иллюстрирует следующая схема: «компонент пищи → рецептор → сигнальный путь → транскрипционный фактор → включение генов» [6, 16] (рис. 3). Рецепторы распознают строго определенную структуру веществ, поэтому схожие по строению компоненты пищи различно воздействуют на организм (например, насыщенные и ненасыщенные жиры). В данной схеме возможны небольшие вариации, например, ядерные рецепторы совмещают в себе функции рецептора и транскрипционного фактора: они распознают различные гидрофобные компоненты еды или их производные (жирные кислоты, витамин D, ретиноевую кислоту, желчные соли и пр.), а затем изменяют активность регулируемых ими генов [17–19].
Пища состоит из белков, углеводов и жиров. Компоненты пищи расщепляются в процессе пищеварения до более простых веществ (аминокислоты, моносахара, жирные кислоты), которые далее транспортируются в клетки и связываются рецепторами. Сигнал от рецептора распространяется по клетке, доходит до ядра и экспрессия генов изменяется. Длительные изменения в экспрессии генов, в конечном счете, сказываются на здоровье и продолжительности жизни. Но обо всем подробнее.
Белки в пищеварительном тракте распадаются до аминокислот, которые затем транспортируются внутрь клеток. В клеточной цитоплазме плавает молекула mTOR (mammalian target of rapamycin), которая активируется высокой концентрацией аминокислот и регулирует многочисленные аспекты метаболизма в клетке. Примечательно, что сигнальный путь mTOR — консервативный биохимический путь, регулирующий старение у животных. Генетические мутации, ослабляющие сигнал mTOR-пути, продлевают жизнь червей, мушек и мышей [20]. Поскольку mTOR активируется аминокислотами, то можно ожидать, что рацион с ограниченным содержанием белков будет благоприятно сказываться на здоровье и долголетии. Действительно, потребление малого количества белков или метионина (незаменимой аминокислоты) повышает продолжительность жизни у модельных животных [21]. У людей диета с низким соотношением белков и углеводов снижает риск развития рака, ожирения и нейродегенеративных заболеваний [22]. Согласно исследованиям, люди пожилого возраста (50–65 лет), получающие из белков более 20% суточных калорий в четыре раза (!) чаще умирают от рака, а уровень их общей смертности на 75% выше по сравнению с людьми, соблюдающими низкобелковую диету (т.е. менее 10% суточных калорий) [23]. Интересно, что корреляция между употреблением растительных белков и уровнем смертности не выявлена. Считается, что это обусловлено аминокислотным составом растительных белков, которые содержат меньше метионина и цистеина [23].
Углеводы в процессе пищеварения расщепляются до моносахаров; самый известный представитель этого класса — глюкоза. Повышение уровня глюкозы в крови вызывает выработку гормона инсулина. Инсулин улавливается рецепторами на поверхности клеток, что приводит к активации сигнального пути IIS (Insulin/Insulin-like grow factor Signaling), который запускает поглощение клетками глюкозы, а также стимулирует клеточный рост и деление. Сигнальный путь IIS тесно переплетен с путем mTOR, соответственно, уровень его активации имеет последствия для здоровья и продолжительности жизни. Мыши, гетерозиготные по рецептору IGF-1 (Insulin-like grow factor) (Igf1r+/−), в среднем, жили на 26% дольше, чем их гомозиготные братья (Igf1r+/+). Что касается людей, то генетические полиморфизмы, снижающие уровень сигнала IIS-пути, ассоциированы с долголетием [23]. Многочисленные исследования демонстрируют, что ограничение калорий у животных снижает уровень IGF в крови; вместе с IGF падает и риск развития атеросклероза, рака и прочих болезней [22]. У людей голодание несколько дней в неделю (потребление менее 25% от суточной нормы калорий) улучшает такие маркеры сердечно-сосудистых заболеваний, как уровень холестерина (ЛПНП) в крови и чувствительность к инсулину* [23].
* — Подробности о механизмах действия низкобелковой диеты и сигнальных путях mTOR и IIS разобраны в статье «Нутригеронтология: питания vs. старение» [24].
Жиры перерабатываются до жирных кислот, моноглицеридов и глицерина. Биохимические эффекты жирных кислот активно исследуются в нутригеномике, так как они запускают множество сигнальных путей, и многие заболевания связаны именно с нарушением липидного обмена. Жирные кислоты можно разделить на два основных класса: ненасыщенные (к которым относятся полиненасыщенные жирные кислоты и транс-жиры) и насыщенные.
Полиненасыщенные жирные кислоты (ПНЖК). ПНЖК содержатся в оливковом масле, семечках, тунце, лососе. ПНЖК необходимы для нормальной работы организма, их употребление благотворно влияет на работу сердечно-сосудистой и нервной систем [25]. Внутри клетки ПНЖК распознаются ядерными рецепторами PPAR (peroxisome proliferator—activated receptors), которые также выполняют функции транскрипционных факторов и регулируют гены метаболизма. Активация PPARα в печени способствует катаболизму жиров в организме (т.е. их утилизации). Также ПНЖК снижают экспрессию генов, вовлеченных в синтез холестерина и жирных кислот. Особенно полезны для организма омега-3-жирные кислоты, которыми богаты рыбий жир, льняное масло и грецкие орехи. Рыбий жир снижает уровень холестерина в крови и печени [26]. Исследования демонстрируют, что ω-3-жирные кислоты (но не ω-6-ЖК) ингибируют рост ободочного рака кишки in vitro и in vivo [27]. Помимо этого, ω-3-жирные кислоты обладают противовоспалительным действием, так как функционируют в качестве субстратов для синтеза противовоспалительного простагландина E3, протектинов и резолвинов, участвующих в рассасывании воспаления и защите клеток [28]. Кроме того, ω-3-жирные кислоты изменяют ацетилирование гистонов и таким образом подавляют действие транскрипционного фактора NF-kB на гены иммунного ответа и апоптоза, которые он регулирует [28].
Транс-жиры. Транс-жиры образуются в пищевой индустрии из ненасыщенных жирных кислот при производстве маргарина, который используется в изготовлении выпечки, крекеров, чипсов и пр. Исследования демонстрируют, что существует прямая зависимость между потреблением транс-жиров и развитием сердечно-сосудистых заболеваний, диабета, ожирения, аллергии, рака груди, а также сокращением периода беременности [29]. В экспериментах, проведенных на мышах, ученые определили, что транс-жиры усиливают в печени экспрессию PGC-1 — ключевого регулятора липидного обмена. Это способствует экскреции липопротеинов низкой плотности в кровь и отложению холестерина в сосудах [30]. Также транс-жиры встраиваются в клеточную мембрану, вызывают воспаление и нарушают работу клеток (рис. 4) [31].
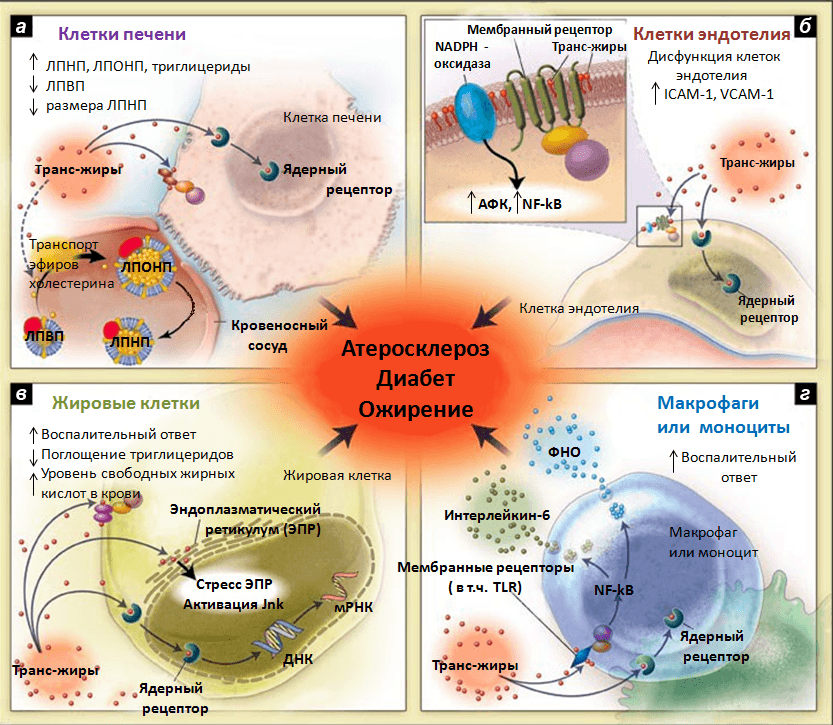
Рисунок 4. Предполагаемые механизмы действия транс-жиров. (а) Транс-жиры изменяют продукцию, секрецию и катаболизм липопротеинов в клетках печени, а также влияют на транспорт эфиров холестерина в липопротеины очень низкой плотности. (б) В эндотелиоцитах увеличивается синтез циркулирующих молекул адгезии и снижается функция NO-синтазы. (в) Под действием транс-жиров изменяется нормальный метаболизм жиров в адипоцитах и усиливается воспалительный ответ. (г) В макрофагах возрастает продукция медиаторов воспаления (интерлейкина-6, фактора некроза опухолей). Перечисленные эффекты транс-жиров подтверждены исследованиями на людях и способствуют атеросклерозу, диабету, отрыву бляшек, внезапной смерти от сердечных патологий. Внутриклеточные механизмы действия транс-жиров точно не установлены. Возможны: изменения в мембранных фосфолипидах клетки, что влияет на функции мембранных рецепторов (таких, как NO-синтаза на эндотелиоцитах или TLR на макрофагах); прямое взаимодействие транс-жирных кислот с ядерными рецепторами, регулирующими транскрипцию генов (например, X рецептором печени); опосредованный или прямой эффект на ЭПР, активация киназы Jnk, которая обычно активируется в ответ на клеточный стресс и регулирует апоптоз, деление клеток, продукцию цитокинов. Предполагаемые механизмы нуждаются в дальнейшем изучении. Рисунок с сайта www.ufrgs.br, адаптирован.
Насыщенные жирные кислоты (НЖК). Основные источники насыщенных жирных кислот — сливочное масло, сыр, мясо, желтки, кокосовое, пальмоядровое масла и масло какао. Существуют данные, что НЖК способствуют воспалению через прямую активацию рецепторов TLR4 (Toll-like receptor) на макрофагах [32]. Рецептор TLR4 — это рецептор врожденного иммунитета, распознающий определенный компонент клеточной стенки бактерий, в состав которого входит липид. Сигнал от TLR4 активирует ключевой транскрипционный фактор иммунного ответа — NFkB. Несмотря на то, что результаты исследований относительно неблагоприятного воздействия НЖК на здоровье противоречивы, Всемирная организация здравоохранения рекомендует сократить долю насыщенных жирных кислот в рационе до 5–10% (от общего количества калорий).
Известно, что одинаковые факторы (идентичные диета и степень физической активности) могут сказаться на метаболизме людей по-разному. Например, недавно было выявлено, что у женщин в зависимости от типа аллеля, потребление ПНЖК способно оказывать противоположные эффекты на уровень липопротеинов высокой плотности (ЛВП) в крови [33]. Соответственно, при проведении нутригеномных исследований надо обязательно учитывать индивидуальные генетические особенности.
Нутригенетика: от генов к пище
Нутригенетика изучает, как вариации в генах отражаются на усвоении и метаболизме пищи и, соответственно, выявляет генетические предрасположенности к заболеваниям. Генетические заболевания подразделяют на моногенные (определяются вариацией в одном гене) и полигенные (определяются комбинацией генов + факторами внешней среды) [36].
К моногенным заболеваниям относят, например, фенилкетонурию, глютеновую болезнь, непереносимость лактозы. Причина таких заболеваний ясна, поэтому внешние проявления предотвратить просто: достаточно исключить из рациона неусваиваемый компонент пищи. Для профилактики полигенных заболеваний — ожирения, диабета II типа, рака, нарушений сердечно-сосудистой системы — необходимо контролировать не только рацион, но и следить за степенью физической активности, уровнем стресса и пр. Тем не менее, накапливающиеся знания из нутригенетики и нутригеномики позволяют индивидуально (в зависимости от генотипа) выявить группы риска и определить, каких продуктов данному человеку стоит избегать, а какими, наоборот, дополнить свое ежедневное меню, чтобы минимизировать риски заболеваний.
Сердечно-сосудистые заболевания (CCЗ). Развитие ССЗ чрезвычайно комплексно, поэтому ученые еще далеки от установления всех факторов рисков и способов их устранения. Однако в генах липидного обмена (генах аполипопротеинов E, A1, A2, A54; PPARs; липоксигеназы-5 и др.) выявлены вариации, у обладателей которых быстрее развивается ССЗ от высококалорийного питания [35]. Также показано, что у людей с медленным метаболизмом кофеина повышается риск сердечных атак при его употреблении [36]. При этом доказан основной риск развития ССЗ — наличие метаболического синдрома, который характеризуется «смертельной четверкой»: повышением артериального давления, уровня сахара и липидов в крови, ожирением. Поэтому главная актуальная задача в этой области — установление молекулярных механизмов общего патологического процесса, который приводит к таким разным метаболическим нарушениям [34].
Рак. Особенности транспорта и метаболизма питательных веществ вносят вклад в развитие (или предотвращение) раковых заболеваний. Например, распространена мутация, снижающая эффективность фермента, необходимого для метилирования ДНК. При недостатке в пище источников метильных групп (фолата и холина), носители такой мутации имеют повышенную вероятность заболеть колоректальным раком. Для таких людей употребление алкоголя — это дополнительный усугубляющий фактор, так как алкоголь снижает абсорбцию фолата и увеличивает его выведение из организма [34]. Употребление красного мяса значительно увеличивает риск развития колоректального рака как у обладателей быстрой N-ацетилтрансферазы, так и у носителей особой комбинации полиморфизмов в гене цитохрома P450 [33, 36]. Обнаружено также, что вероятность онкологических заболеваний возрастает при мутации в гене одного из типов глутатионтрансфераз (ферментов, участвующих в детоксикации), и постоянное поступление в организм токсинов (при курении и др.) опасно для людей с подобной мутацией. А поедание капусты и прочих крестоцветных, наоборот, будет крайне полезно, так как они содержат вещества, увеличивающие активность глутатионтрансфераз [34].
Ожирение. Определенный вариант гена FTO (fat mass- and obesity-associated gene) ассоциирован у людей с ожирением и диабетом. Во время проведения исследований выяснилось, что при неограниченном доступе к еде дети с таким вариантом FTO склонны потреблять более калорийную пищу. Эффект подобного генетического варианта легко модулируется физической активностью и сбалансированным питанием.
Несмотря на возможные генетические предрасположенности к ожирению, диабету, сердечно-сосудистым заболеваниям и раку, показано, что факторы окружающей среды играют существенную роль при развитии вышеперечисленных патологий [7]. Поэтому ВОЗ были составлены базовые рекомендации для поддержания здоровья: употребление разнообразных фруктов и овощей в течении дня, снижение потребления насыщенных и транс-жиров, копченостей, соленой пищи; умеренное употребление алкоголя; активный образ жизни; поддержание нормального веса. Различные исследования подтвердили обратную зависимость между употреблением овощей и фруктов и частотой онкологических заболеваний [37, 38]. Кроме того, накапливающиеся данные о благотворном влиянии на здоровье и долголетие рациона с низким содержанием животных белков уже сегодня заставляют диетологов выстраивать новую систему сбалансированного питания. Однако для полноценного представления о механизмах влияния составляющих пищи (а также их комбинаций) на организм, и возможных разбросах такого влияния среди человеческой популяции предстоит еще сделать много работы. Существует ряд проблем, которые необходимо решить для получения достоверной информации и внедрения нутригеномики/нутригенетики в повседневную жизнь.
Проблемы
Отдельно взятый прием пищи оказывает слабое влияние на организм, поэтому при проведении нутригеномных исследований очень важна длительность употребления нутриентов, что усложняет проведение экспериментов. Для анализа изменений в экспрессии генов и метаболизма клетки используются следующие методы: эпигенетический анализ и анализ клеточных мРНК (транскриптома), белков (протеома) и метаболитов (метаболома) (рис. 5). К сожалению, на сегодняшний день методы получения протеома и метаболома дороги и развиты недостаточно, а количество мРНК не всегда пропорционально количеству белка в клетке и не дает информации об активности белка. Кроме того, для исследований требуется достаточно большое количество биологического материала, поэтому анализируется, в основном, кровь, в частности, белые кровяные клетки (жировая и мышечная ткани — на втором месте), но до сих пор неизвестно, насколько точно они отражают ранние нарушения в метаболизме [39].
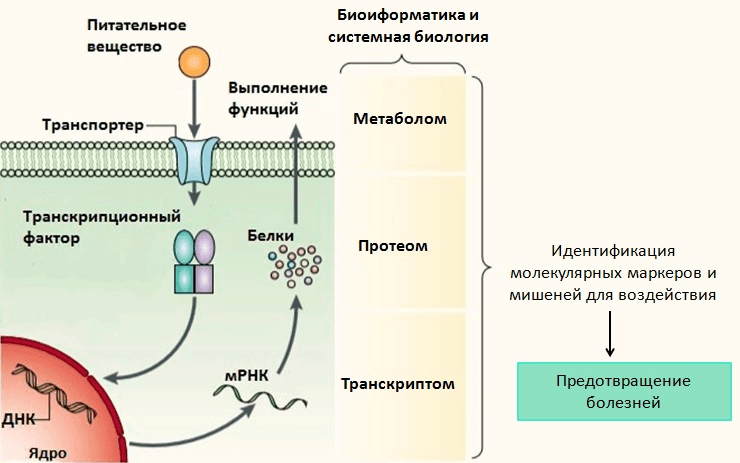
Рисунок 5. Нутригеномные методы исследования. Рисунок из [6], адаптирован.
Несмотря на то, что пока не накоплено достаточного объема достоверной информации для внедрения нутригеномики и нутригенетики в повседневную жизнь, уже существуют компании, предлагающие нутригенетические тесты (правительство США выпустило отчет об опасности и недостоверности таких тестов). Такие компании вызывают сомнения у людей о научной релевантности таких областей, как нутригеномика и нутригенетика, что мешает их распространению и внедрению в общество.
Перспективы
Ожидается, что вклад нутригеномики и нутригенетики в здравоохранение в следующем десятилетии будет очень значительным. Установление молекулярных механизмов взаимодействия «пища—гены» и выявление ранних маркеров нарушений в метаболизме позволит проводить эффективное превентивное лечение. Планируется составлять индивидуальный план питания на основе особенностей метаболизма и генетических предрасположенностей (рис. 6). Продукты питания будут проверяться не только на безопасность, но и на эффективность их действия на организм.
Статья с сайта Биомолекула
http://biomolecula.ru/content/1905
